La leucèmia mielomonocítica juvenil
La leucèmia és el càncer més freqüent en nens. Afecta més de 350 nens l’any al nostre país, dels quals un terç tenen menys de 4 anys. La leucèmia representa el 30 % de tots els càncers pediàtrics, i la leucèmia limfoblàstica aguda B és la forma més comuna en nens (80 % dels casos). La leucèmia mieloide aguda afecta aproximadament a un 20 % dels pacients de leucèmia en edat pediàtrica, especialment abans dels 2 anys. La leucèmia mielomonocítica juvenil és una forma molt poc freqüent i greu de leucèmia que afecta a menys de 10 nens l’any en el nostre país.
La informació proporcionada a www.fcarreras.org serveix per donar suport, no reemplaçar-la, a la relació que existeix entre els pacients/visitants d’aquest lloc web i del seu metge.
Informació avalada per… ![]()
Informació proporcionada per la Dra. Laura Belver, investigadora en leucèmia mielomonocítica juvenil de l’Institut d’Investigació contra la Leucèmia Josep Carreras
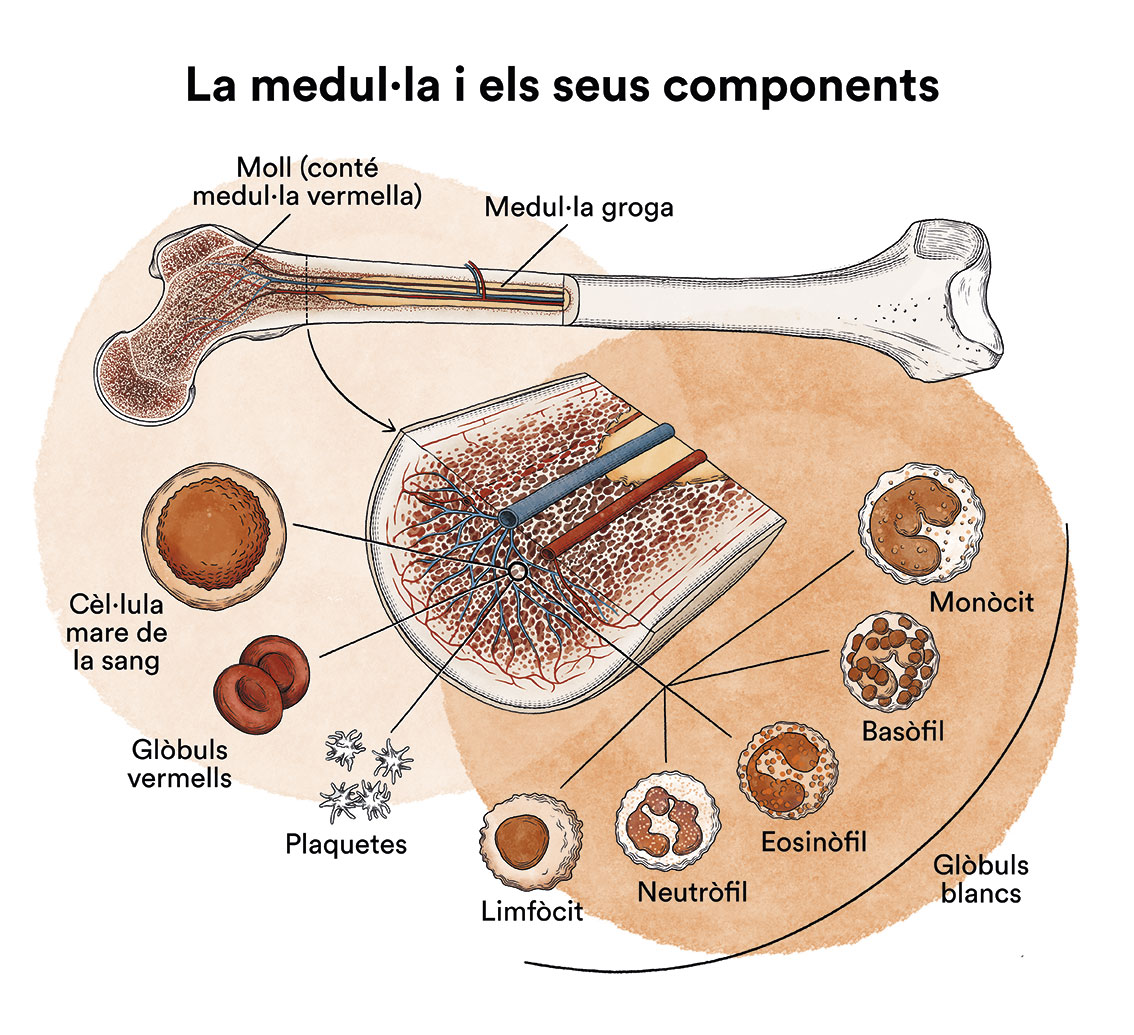
Què és la leucèmia, la medul·la òssia i quins són els tipus de cèl·lules sanguínies?
La leucèmia és un tipus de càncer de les cèl·lules de la sang i de la medul·la òssia. Vegeu apartat Leucèmia, medul·la òssia i cèl·lules sanguínies.
Què es la leucèmia mielomonocítica juvenil?
 La leucèmia mielomonocítica juvenil (LMMJ) succeeix quan les cèl·lues mare o cèl·lues progenitores de la medul·la òssia, responsables de la generació de totes les cèl·lules sanguínies, es comporten d’una manera anormal, proliferant de forma descontrolada i produint grans nombres de monòcits en la sang que s’infiltren en diferents òrgans del pacient.
La leucèmia mielomonocítica juvenil (LMMJ) succeeix quan les cèl·lues mare o cèl·lues progenitores de la medul·la òssia, responsables de la generació de totes les cèl·lules sanguínies, es comporten d’una manera anormal, proliferant de forma descontrolada i produint grans nombres de monòcits en la sang que s’infiltren en diferents òrgans del pacient.
La leucèmia mielomonocítica juvenil és un tipus de leucèmia molt poc freqüent, que presenta una incidència de només 1,2 casos per cada milió de nens i nenes de menys de 14 anys; és més freqüent en homes (2 de cada 3 pacients). Cada any es diagnostiquen a l’Estat espanyol entre 5 i 10 casos de LMMJ, en la seva majoria nens i nenes de menys de 2 anys, encara que també pot presentar-se en edats més avançades, especialment en pacients que pateixin neurofibromatosis tipus 1. Aproximadament el 10 % dels casos de LMMJ succeeixen en nadons de menys de 3 mesos.
Quines són les causes de la leucèmia mielomonocítica juvenil?
 Les causes específiques que originen la leucèmia mielomonocítica juvenil no es coneixen. No obstant això, s’han identificat cinc gens que presenten mutacions en les cèl·lules de la medul·la òssia del 90 % dels pacients de LMMJ. Aquestes mutacions es consideren els desencadenants de la malaltia. En 10 % restant dels pacients, la mutació genètica que actua com a promotora de la leucèmia encara es desconeix.
Les causes específiques que originen la leucèmia mielomonocítica juvenil no es coneixen. No obstant això, s’han identificat cinc gens que presenten mutacions en les cèl·lules de la medul·la òssia del 90 % dels pacients de LMMJ. Aquestes mutacions es consideren els desencadenants de la malaltia. En 10 % restant dels pacients, la mutació genètica que actua com a promotora de la leucèmia encara es desconeix.
Algunes malalties del desenvolupament, com ara la neurofibromatosi tipus 1 i la síndrome CBL, poden fer que un nen sigui més procliu a desenvolupar una leucèmia mielomonocítica juvenil.
La leucèmia, com altres tipus de càncer, no és contagiosa. Vegeu apartat Leucèmia, medul·la òssia i cèl·lules sanguínies.
Com es classifica la leucèmia mielomonocítica juvenil?
La leucèmia mielomonocítica juvenil és molt heterogènia i ha estat sempre difícil de classificar. Al llarg del temps se l’ha denominat leucèmia mieloide crònica juvenil, leucèmia mielomonocítica crònica infantil o síndrome de monosomia 7 infantil. Vegeu classificació LMMJ.
Quins són els símptomes de la leucèmia mielomonocítica juvenil?
La presentació clínica de la LMA és variable i, en general, els símptomes en el diagnòstic es deuen a la infiltració de les cèl·lules leucèmiques de la medul·la òssia i altres òrgans, i dificulten el seu correcte funcionament.
Això pot ocasionar:
- Cansament, debilitat, mareig i pal·lidesa, a conseqüència del nombre reduït de glòbuls vermells en la sang (anèmia)
- Aparició d’hematomes o petites taques rosades en la pell (petèquies), així com altres tipus de sagnats com ara hemorràgies nasals o de genives, a causa del nombre reduït de plaquetes en la sang.
- Febre i infeccions que no evolucionen bé (bronquitis, amigdalitis…), per la generació deficient de les cèl·lules del sistema immunològic.
- De vegades succeeix la inflamació dolorosa dels ganglis limfàtics, el fetge o la melsa, a causa de l’acumulació de cèl·lules leucèmiques.
- Dolor o sensació de plenitud en les costelles
- Tos seca
- Pèrdua de gana i insuficiències del creixement

Al l’inici de la malaltia, tots aquests símptomes es poden confondre amb els d’una infecció vírica; per aquesta raó, aconseguir el diagnòstic final del pacient pot prolongar-se durant varies setmanes. No obstant això, en general, això no afecta les opcions de curació del nen o nena.
Com es diagnostica la leucèmia mielomonocítica juvenil?
A part dels estudis bàsics en sang i medul·la òssia comuns per a tot tipus de leucèmia (morfologia, recompte, immunofenotip), les anàlisis citogenètiques (per detectar anomalies cromosòmiques) i moleculars (per detectar mutacions) són fonamentals per tipificar i classificar la malaltia. Determinades alteracions genètiques poden predir l’agressivitat de la malaltia i el risc de recaiguda del pacient. Tots els pacients amb sospita de leucèmia mielomonocítica juvenil se sotmeten a una anàlisis genètica en la qual es comparen les seves cèl·lules tumorals amb les seves cèl·lules normals. En més del 90 % dels pacients amb leucèmia mielomonocítica juvenil es detecten mutacions en un d’aquests cinc gens: PTPN11, KRAS, NRAS, NF1 o CBL. Tots aquests gens pertanyen a l’anomenada via de senyalització RAS, que controla el creixement i la divisió cel·lular. Les mutacions que es troben en la leucèmia mielomonocítica juvenil produeixen la hiperactivació d’aquesta via, la qual cosa fa que les cèl·lules tumorals creixin de manera descontrolada.
Quin és el tractament de la leucèmia mielomonocítica juvenil?
Actualment no existeix un tractament específic per tractar la leucèmia mielomonocítica juvenil. L’únic tractament que ha demostrat poder curatiu és el trasplantament de progenitors hematopoètics (trasplantament de medul·la òssia) d’un donant HLA compatible. No obstant això, és una teràpia no exempta de riscos i complicacions i, aproximadament un 30 % dels nens recauen després del trasplantament.
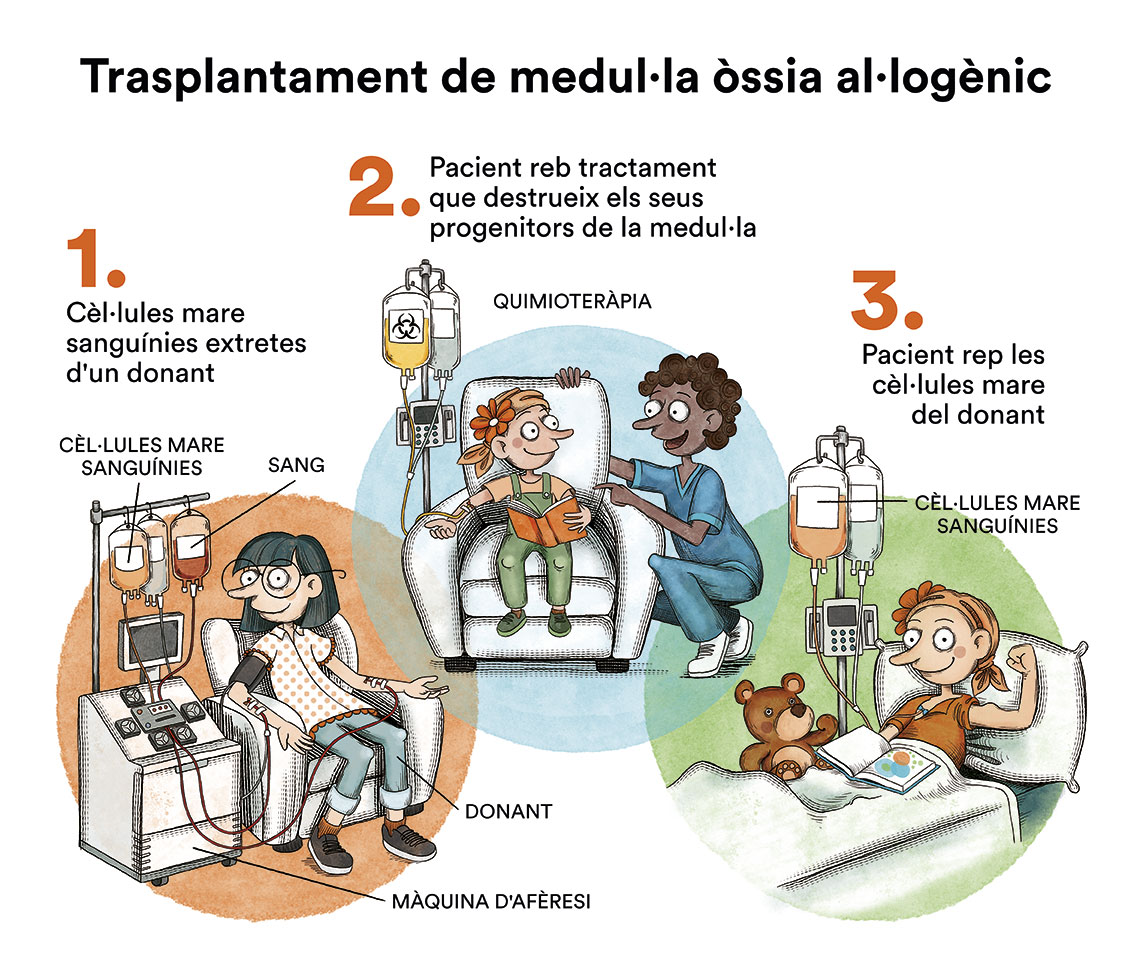
Sense tractament, la leucèmia mielomonocítica juvenil progressa ràpidament. La quimioteràpia (l’ús de fàrmacs especials per matar les cèl·lules canceroses) es pot utilitzar per controlar de forma temporal la leucèmia mielomonocítica juvenil i preparar el pacient per al trasplantament, però no com a teràpia curativa. Un dels tractaments tradicionalment utilitzats abans de realitzar el trasplantament de medul·la és la combinació dels medicaments quimioterapèutics busulfan, ciclofosfamida i melfalan. No obstant això, recentment s’ha aprovat amb la mateixa finalitat l’ús d’azacitidina, que pot ser administrada en pacients pediàtrics a partir d’un mes d’edat. Els pacients que aconsegueixen una remissió temporal de la leucèmia en aquests cicles de quimioteràpia tindran un millor pronòstic a llarg termini. Segons la Leukemia and Lymphoma Society, el trasplantament es recomana per a tots els nens amb mutacions en els gens NF1 i PTPN11. Malgrat això, l’enfocament d’“espera vigilant” s’adopta en els pacients amb mutacions en el gen CBL i alguns pacients amb mutacions en NRAS, en els quals la severitat de la malaltia és menys acusada i en ocasions pot arribar a resoldre’s sense intervenció. Vegeu classificació LMMJ.

Degut a les poques alternatives de tractament existents per a la leucèmia mielomonocítica juvenil, existeix la possibilitat que l’equip clínic responsable a càrrec del nen o nena pugui proposar la seva inclusió en assajos clínics amb nous medicaments en fase d’investigació. És molt recomanable que el nen o nena sigui tractat en un centre de referència amb hematòlegs amb experiència en el tractament d’aquesta malaltia.
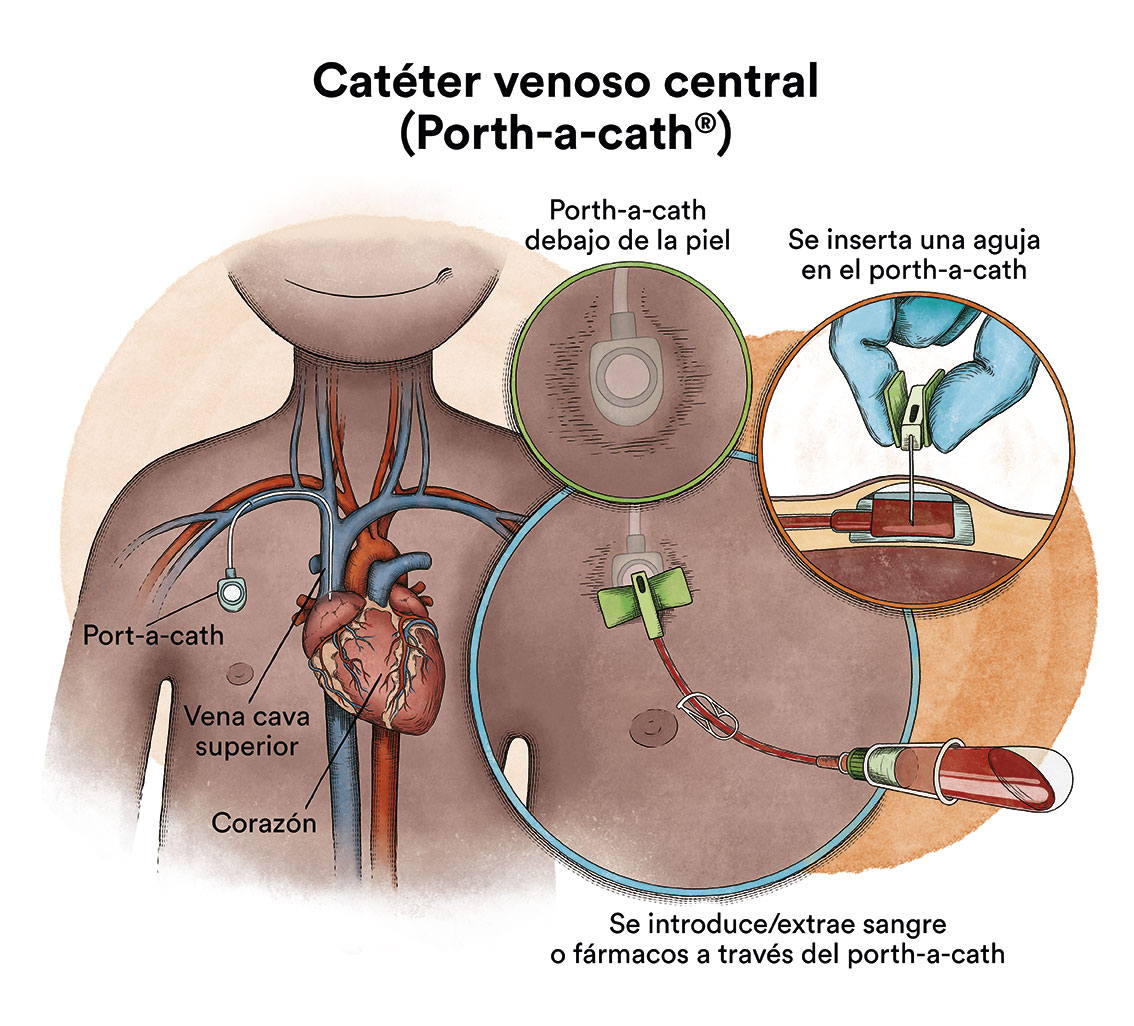
Quan la quimioteràpia s’administra per via intravenosa, per evitar punxar repetidament una vena, s’utilitza un dispositiu especial anomenat catèter (contingut en espanyol). El catèter s’introdueix en una vena gran i permet tant l’administració de medicaments com l’extracció de sang per a anàlisi, per així evitar realitzar repetides puncions al menut.
Existeix un tipus de catèter, anomenat port-a-cath, que s’uneix a un reservori rodó de plàstic o metall que queda sota la pell del tòrax. El port-a-cath és molt pràctic en nens perquè al quedar sota de la pell no permet que el nen nena se l’arrenqui, es més difícil que s’infecti que altres tipus de catèter i permet que el nen es banyi.
Quines probabilitats tenen de curar-se els nens amb leucèmia mielomonocítica juvenil?
Les probabilitats de curació venen determinades per les característiques del pacient, de la malaltia (alteracions genètiques/moleculars), el tractament que s’administri per la resposta que es presenti.
Prop del 50 % dels pacients aconsegueix la remissió completa a llarg termini després del trasplantament de medul·la òssia. S’ha de dir que aquesta teràpia no està exempta de complicacions. Entre el 30 i el 40 % dels nens amb leucèmia mielomonocítica juvenil sotmesos a tractament i trasplantament al·logènic recaurà dins del primer any. De vegades, per a aquests nens es planteja un segon trasplantament de medul·la òssia.
Nous tractaments contra la leucèmia mielomonocítica juvenil
La LMMJ ha representat històricament un desafiament clínic degut principalment al nombre limitat d’opcions terapèutiques per al seu tractament i a l’alt risc de mortalitat dels nens amb les formes més agressives de la malaltia. Tot i que el trasplantament de medul·la òssia és en l’actualitat l’únic tractament curatiu, els avanços en la investigació d’aquesta malaltia han permès identificar noves estratègies terapèutiques que s’estan ja utilitzant en els pacients o explorant en diferents assajos clínics:
- Agents hipometilants: Alguns pacients de LMMJ presenten alts nivells de metilació en el seu ADN associats amb les formes més agressives de la malaltia. La metilació és una modificació química que succeeix en l’ADN i controla l’activitat dels gens. Per contrarestar aquesta hipermetilació, recentment s’ha aprovat l’ús d’azacitidina (Vidaza®) per al tractament dels pacients de LMMJ. Aquest medicament entra dins del grup dels anomenats agents hipometilants, capaços de reduir la metilació de l’ADN. En l’actualitat s’estan estudiant les possibles combinacions de l’Azacitidina amb altres fàrmacs per millorar els resultats.
- Inhibidors de MEK: La majoria dels pacients amb leucèmia mielomonocítica juvenil presenten mutacions en gens que produeixen la hiperactivació de la via de senyalització RAS, que controla la proliferació cel·lular i produeix un creixement descontrolat de les cèl·lules tumorals. Per aquest motiu, el bloqueig de la via RAS amb els anomenats inhibidors MEK és una de les estratègies terapèutiques que més s’està investigant actualment per a casos de LMMJ en recaiguda i/o refractaris. Entre aquests inhibidors es troben els fàrmacs com el trametinib (Mekinist®).
Seguiment
Després de completar el tractament, el nen seguirà controls periòdics pel seu metge hematòleg i per altres especialistes en cas que sigui necessari. Els controls es realitzen per avaluar una possible recaiguda i per fer un seguiment i un tractament de les possibles complicacions a llarg termini. Aquests controls es van espaiant progressivament fins fer-se una vegada a l’any. És recomanable fer un seguiment com a mínim anual a llarg termini per poder detectar aviat i poder tractar, si apareixen, les seqüeles del tractament o de la leucèmia.
Enllaços d'interès sobre temes mèdics relacionats amb la leucèmia mielomonocítica juvenil
- La leucèmia mielomonocítica juvenil. St JudeChildren’s Research Hospital
- La leucèmia mielomonocítica crònica i la leucèmia mielomonocítica juvenil. Leukeamia & Lymphoma Research
Enllaços d'interès sobre altres temes relacionats amb la leucèmia mielomonocítica juvenil
MATERIALS LEUCÈMIA INFANTIL
- Els nadons també tenen leucèmia. Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- Leucèmia infantil. Els petits imparables. Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- Joc retallable Medulín. Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
La Fundació Josep Carreras disposa d’un conte “El nadó forçut” dirigit a nens o germans que pateixen leucèmia. Està especialment dirigit a nens fins als 6 anys. Si el vols demanar, pots enviar-nos un correu electrònic a imparables@fcarreras.es.
TRASPLANTAMENT DE MEDUL·LA ÒSSIA
- Guia del Trasplantament de Medul·la Òssia. Fundació Josep Carreras (contingut en espanyol)
- Què és l’HLA i com funciona? Fundació Josep Carreras (contingut en espanyol)
- La Malaltia Empelt contra Receptor. Fundació Josep Carreras (contingut en espanyol)
- Història del Trasplantament de Medul·la Òssia. Fundació Josep Carreras (contingut en espanyol)
- Com es realitza la cerca d’un donant compatible anònim? Fundació Josep Carreras (contingut en espanyol)
MANUALS DE SUPORT
- Com enfrontar-se a la leucèmia i el limfoma en nens? Leukemia & Lymphoma Society.
- VIURE APRENENT. Protocol d’actuació per a alumnes amb càncer AFANION.
- Guia de suport per a pares de nens oncològics ASION.
- Guia per a joves i adolescents amb càncer ASION.
- Alumnat amb càncer. Guia per a docents ASION.
- La importància del comportament dels pares quan un nen té càncer ASION.
- El meu fill té càncer. Què faig? FARO.
ALIMENTACIÓ
- Com mantenir una alimentació saludable durant el tractament? Fundació Josep Carreras (contingut en espanyol)
- “Buon profit”. Consells dietètics durant el tractament AFANION.
- “Les receptes màgiques de Jabel”. Isabel Rojas Murcia, Carolina Mangas Gallardo.
ALTRES
- Informació sobre els efectes a llarg termini i tardans del tractament per a la leucèmia o el limfoma en els nens Leukemia & Lymphoma Society.
- El meu germà té càncer Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- L’escola en un hospital Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- Educant il·lusions. Guia per a la intervenció psicoeducativa en nens i adolescents amb càncer FARO.
- El càncer en l’adolescència Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- Documental “La leucèmia i els adolescents” Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- Documental “Els nadons també tenen leucèmia” Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- 7 formes de posar-se un mocador Fundació Josep Carreras contra la leucèmia. (contingut en espanyol)
- Conte “La princesa Luzie i els cavallers de la quimio’ ASPANAFOA.
- Conte “Anem a quimioteràpia’.
- Conte “Anem a radioteràpia’.
- Conte “Gasparín Súper Quimio” Federación Española de Padres de Niños con Cáncer.
- Vídeo “Charlie Brown i la leucèmia”.
- Conte “El Toby i la màquina voladora”.
- Conte “La fada de les estrelles” AECC.
- Conte “La Lina, la petita oreneta” Osakidetza.
Enllaços d'interès: entitats locals (recursos i serveis)
Totes aquestes organitzacions són externes a la Fundació Josep Carreras.
ANDALUSIA
ARAGÓ
ASTÚRIES
CASTELLA-LA MANXA
CASTELLA I LLEÓ
CATALUNYA
COMUNITAT VALENCIANA
EXTREMADURA
GALÍCIA
ILLES BALEARS
ILLES CANÀRIES
LA RIOJA
MADRID
- AAA (asociación de adolescentes y Adultos Jóvenes con Cáncer)
- ASION
- FUNDACIÓN CAICO
- FUNDACIÓN ALADINA
- FUNDACIÓN UNOENTRECIENMIL
MÚRCIA
NAVARRA
PAÍS BASC
Suport i ajuda
Et convidem també a seguir-nos a les nostres xarxes socials principals (Facebook, Twitter i Instagram) on sovint compartim testimonis de superació.Si resideixes a l’Estat espanyol, també pots posar-te en contacte amb nosaltres enviant-nos un correu electrònic a imparables@fcarreras.es perquè t’ajudem a posar-te en contacte amb altres persones que han superat aquesta malaltia.
* D’acord amb la Llei 34/2002 de Serveis de la Societat de la Informació i el Comerç Electrònic (LSSICE), la Fundació Josep Carreras contra la Leucèmia informa que tota la informació mèdica disponible a www.fcarreras.org ha estat revisada i acreditada pel Dr. Enric Carreras Pons, Col·legiat núm. 9438, Barcelona, Doctor en Medicina i Cirurgia, Especialista en Medicina Interna, Especialista en Hematologia i Hemoteràpia i Consultor sènior de la Fundació; i per la Dra. Rocío Parody Porras, Col·legiada núm. 35205, Barcelona, Doctora en Medicina i Cirurgia, Especialista en Hematologia i Hemoteràpia i adscrita a la Direcció mèdica del Registre de Donants de Medul·la Òssia (REDMO) de la Fundació).
Informació revisada al novembre de 2023.


